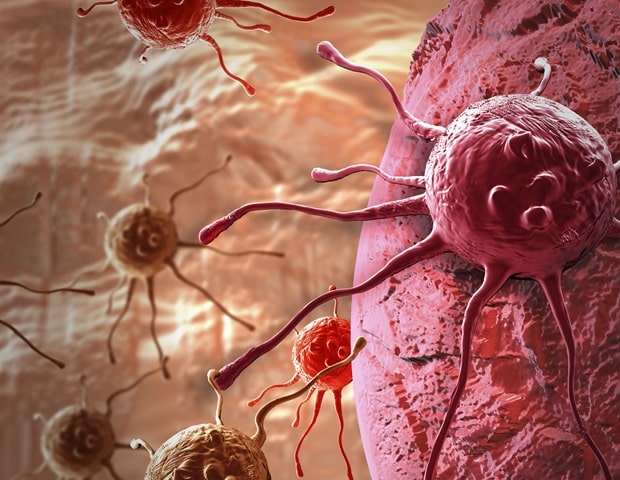
Pacjenci z zaawansowanym stadium nowotworu często muszą przechodzić przez liczne rundy różnych terapii, które mogą wywołać niepożądane skutki uboczne, a czasami nie przynoszą oczekiwanych rezultatów. W odpowiedzi na te wyzwania, naukowcy z MIT opracowali innowacyjne mikroskopijne cząsteczki, które mogą być implantowane bezpośrednio w miejscu guza, dostarczając jednocześnie dwie formy terapii: ciepło oraz chemioterapię.
Nowatorskie podejście do leczenia nowotworów
Wprowadzenie tego rozwiązania może zminimalizować skutki uboczne często występujące przy tradycyjnej chemioterapii podawanej dożylnie. Co więcej, synergiczne działanie obu form terapii może wydłużyć życie pacjenta bardziej niż stosowanie jednej z metod oddzielnie. W badaniach przeprowadzonych na myszach, nowatorska terapia wykazała znaczne efekty, całkowicie eliminując guzy u większości zwierząt i znacząco przedłużając ich przeżywalność.
Jednym z głównych zastosowań tej technologii mogłoby być leczenie szybko rosnących guzów, które są trudne do kontrolowania innymi metodami. Zgodnie z badaniami, nowa metoda mogłaby dać pacjentom więcej czasu, a także poprawić jakość życia w okresie leczenia.
Dwuskładnikowa terapia
Pacjenci z zaawansowanymi guzami często poddawani są kombinacji różnych terapii, takich jak chemioterapia, operacja czy radioterapia. Fototerapia, będąca nowszą metodą, wykorzystuje cząsteczki, które po zaimplantowaniu lub wstrzyknięciu są podgrzewane przy użyciu lasera, co pozwala na niszczenie komórek nowotworowych bez uszkadzania okolicznych tkanek.
Obecne podejścia do fototerapii w badaniach klinicznych często wykorzystują nanocząsteczki złota, które emitują ciepło pod wpływem światła bliskiej podczerwieni. Zespół z MIT postanowił zintegrować fototerapię z chemioterapią, aby zwiększyć skuteczność terapii i zredukować obciążenie dla pacjenta. Do tego celu wybrali nieorganiczny materiał – siarczek molibdenu, który efektywnie przekształca światło lasera w ciepło, co pozwala na użycie niskiej mocy laserów.
Aby stworzyć mikropartikel dostarczający obie terapie, naukowcy połączyli nanowarstwy siarczku molibdenu z doxorubicyną, czyli lekiem hydrofilowym, lub violaceiną, lekiem hydrofobowym. Te składniki zostały zmieszane z polimerem zwanym polikaprolaktonem, a następnie wysuszone do postaci filmu, który można formować w mikroskopijne cząstki o różnych kształtach i rozmiarach.
Proces leczenia
W badaniach naukowcy stworzyli cząstki o kształcie kostki, o szerokości około 200 mikrometrów. Po wstrzyknięciu bezpośrednio w miejsce guza, cząsteczki pozostają tam przez cały okres leczenia. Podczas każdej sesji, zewnętrzny laser bliskiej podczerwieni jest używany do podgrzania cząstek, co pozwala na lokalne oddziaływanie na tkanki.
Jedną z zalet tej platformy jest możliwość aktywowania jej na żądanie, co oznacza, że po jednokrotnym podaniu cząstek do guza, można wielokrotnie uruchamiać terapię przy użyciu lasera, osiągając jednocześnie efekt termicznej ablacjii komórek nowotworowych oraz uwalniania leku. Naukowcy wykorzystali algorytmy uczenia maszynowego, aby zoptymalizować parametry terapii, takie jak moc lasera, czas naświetlania oraz stężenie środka fototerapeutycznego.
W optymalnym scenariuszu laser działa przez około trzy minuty. W tym czasie cząsteczki rozgrzewają się do temperatury około 50°C, co wystarcza do zniszczenia komórek nowotworowych. W tej temperaturze polimerowa matryca cząstki zaczyna się topić, uwalniając niektóre z zawartych w niej leków chemioterapeutycznych.
Całkowite usunięcie guzów
Innowacyjna terapia została przetestowana na myszach, którym wszczepiono agresywny typ komórek nowotworowych pochodzący z potrójnie negatywnego raka piersi. Po utworzeniu się guzów, naukowcy wszczepili około 25 mikroskopijnych cząstek w każdy guz, a następnie przeprowadzili terapię laserową trzykrotnie, z trzydniowymi odstępami między sesjami.
Wyniki były obiecujące – guzy zostały całkowicie wyeliminowane, a myszy przeżyły znacznie dłużej niż te, które otrzymały jedynie chemioterapię, samą fototerapię lub nie były leczone. Myszom, które przeszły wszystkie trzy cykle terapii, udało się uzyskać znacznie lepsze wyniki niż tym, które otrzymały jedynie pojedynczy zabieg laserowy.
Polimer użyty do stworzenia cząstek jest biokompatybilny i został już zatwierdzony przez FDA do użycia w urządzeniach medycznych. Naukowcy mają nadzieję, że kolejnym krokiem będzie testowanie tych cząstek na większych modelach zwierząt, z zamiarem przeprowadzenia badań klinicznych na ludziach. Jest to technologia, która mogłaby znaleźć zastosowanie w leczeniu wszelkich typów stałych guzów, w tym guzów przerzutowych.
Perspektywy na przyszłość
Opracowanie tej nowej technologii może być przełomem w leczeniu zaawansowanych, szybko rosnących nowotworów, zwłaszcza u pacjentów, dla których tradycyjne metody leczenia nie przynoszą oczekiwanych rezultatów. Dzięki połączeniu dwóch form terapii – fototerapii i chemioterapii – możliwe jest bardziej precyzyjne i mniej obciążające dla organizmu podejście do terapii nowotworowej.
Następne kroki w badaniach nad tą technologią mogą prowadzić do szerokiego zastosowania nowej metody w leczeniu różnych nowotworów, co z kolei mogłoby poprawić jakość życia pacjentów oraz zwiększyć ich szanse na dłuższe przeżycie.